Lupin Pharmaceuticals, kullanıcılar için beklenmedik gebeliklere yol açabilecek etkinliğinin azalması nedeniyle iki parti oral doğum kontrolü Tydemy’yi geri çağırdı.
FDA, üreticilerin oral kontrasepsiyonun düşük seviyede askorbik asit, üründe bir bileşen ve yüksek seviyelerde “bilinen bir safsızlık” içerdiğini fark etmesinden sonra hapların gönüllü olarak geri çağrıldığını söyledi.
Şirket, düşük askorbik asit seviyelerinin “potansiyel olarak beklenmedik hamilelikle sonuçlanabilecek ürünün etkinliğini etkileyebileceğini” söyledi. Ancak FDA, “bu ürünün kullanılmasıyla ilgili herhangi bir olumsuz olay” raporu almadıklarını kaydetti.
Lupin Pharmaceuticals, Inc. 2 Parti Tydemy’nin Ülke Çapında Gönüllü Olarak Geri Çağırılmasını Düzenledi (FDA)

Federal Gıda ve İlaç İdaresi, Tydemy’nin geri çağrılan partilerinin hamilelikle sonuçlanabileceği konusunda uyardı. (iStock)
Östrojen ve progestin reçeteli bir doğum kontrol hapı olan Tydemy haplarının geri çağrılan partileri L200183 ve L201560 lotlarıdır ve 3 Haziran 2022’den 31 Mayıs 2023’e kadar ABD’deki eczaneler tarafından dağıtılmıştır. etiketin yan tarafı.
AI BEBEKLER: YENİ TEKNOLOJİ DOĞURMA DOKTORLARININ IVF İÇİN EN İYİ EMBRİYOLARI SEÇMELERİNE YARDIMCI OLUYOR
FDA’ya göre, toplam 4.179 kutu oral doğum kontrolü geri çağrıldı.
Halihazırda çok sayıda ilaç kullanmakta olan kişilerin haplarını almaya devam etmeleri, ancak doktorlarından hemen bir alternatif aramaları istenmektedir.
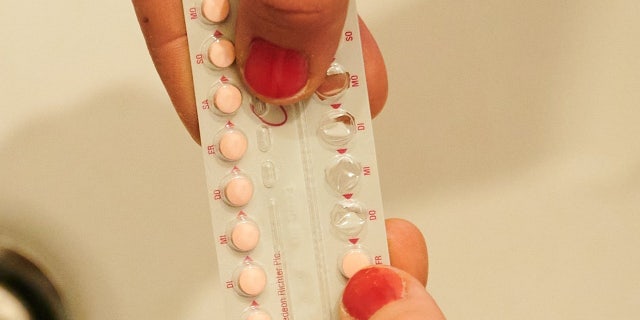
Bir kadın doğum kontrol hapının aylık paketinden bir sonraki hapı alır. (Annette Riedl/Getty Images aracılığıyla resim ittifakı)
SAĞLIK BÜLTENİMİZE ÜYE OLMAK İÇİN TIKLAYINIZ
Bu, Lupin İlaç’ın ilk gönüllü geri çağırması değil.
Geçen yılın Aralık ayında, Lupin bir parti ürünü geri çağırdı. 20 miligram Quinapril Tablet USP ve bir nitrozamin safsızlığının potansiyel varlığı nedeniyle üç parti 40 miligram Quinapril Tablet USP.
HABERLER SUNULDU
Sarah Rumpf-Whitten, Haberler Digital’in son dakika haber ekibinde bir yazardır. Ona Twitter’da @s_rumpfwhitten adresinden ulaşabilirsiniz.
FDA, üreticilerin oral kontrasepsiyonun düşük seviyede askorbik asit, üründe bir bileşen ve yüksek seviyelerde “bilinen bir safsızlık” içerdiğini fark etmesinden sonra hapların gönüllü olarak geri çağrıldığını söyledi.
Şirket, düşük askorbik asit seviyelerinin “potansiyel olarak beklenmedik hamilelikle sonuçlanabilecek ürünün etkinliğini etkileyebileceğini” söyledi. Ancak FDA, “bu ürünün kullanılmasıyla ilgili herhangi bir olumsuz olay” raporu almadıklarını kaydetti.
Lupin Pharmaceuticals, Inc. 2 Parti Tydemy’nin Ülke Çapında Gönüllü Olarak Geri Çağırılmasını Düzenledi (FDA)

Federal Gıda ve İlaç İdaresi, Tydemy’nin geri çağrılan partilerinin hamilelikle sonuçlanabileceği konusunda uyardı. (iStock)
Östrojen ve progestin reçeteli bir doğum kontrol hapı olan Tydemy haplarının geri çağrılan partileri L200183 ve L201560 lotlarıdır ve 3 Haziran 2022’den 31 Mayıs 2023’e kadar ABD’deki eczaneler tarafından dağıtılmıştır. etiketin yan tarafı.
AI BEBEKLER: YENİ TEKNOLOJİ DOĞURMA DOKTORLARININ IVF İÇİN EN İYİ EMBRİYOLARI SEÇMELERİNE YARDIMCI OLUYOR
FDA’ya göre, toplam 4.179 kutu oral doğum kontrolü geri çağrıldı.
Halihazırda çok sayıda ilaç kullanmakta olan kişilerin haplarını almaya devam etmeleri, ancak doktorlarından hemen bir alternatif aramaları istenmektedir.

Bir kadın doğum kontrol hapının aylık paketinden bir sonraki hapı alır. (Annette Riedl/Getty Images aracılığıyla resim ittifakı)
SAĞLIK BÜLTENİMİZE ÜYE OLMAK İÇİN TIKLAYINIZ
Bu, Lupin İlaç’ın ilk gönüllü geri çağırması değil.
Geçen yılın Aralık ayında, Lupin bir parti ürünü geri çağırdı. 20 miligram Quinapril Tablet USP ve bir nitrozamin safsızlığının potansiyel varlığı nedeniyle üç parti 40 miligram Quinapril Tablet USP.
HABERLER SUNULDU
Sarah Rumpf-Whitten, Haberler Digital’in son dakika haber ekibinde bir yazardır. Ona Twitter’da @s_rumpfwhitten adresinden ulaşabilirsiniz.
