Halk sağlığı kurumunun Çarşamba günü yaptığı duyuruya göre, Gıda ve İlaç İdaresi (FDA), ABD’de kullanılmak üzere ilk solunum sinsityal virüsü (RSV) aşısını onayladı.
Arexvy adı verilen ilacın, 60 yaş ve üzerindeki kişilerde bir hastalık olan RSV’yi önlemek için kullanılması onaylanmıştır. alt solunum yolu hastalığı.
FDA Biyoloji Merkezi Direktörü Dr. Peter Marks, “Yaşlı yetişkinler, özellikle kalp veya akciğer hastalığı veya zayıflamış bağışıklık sistemleri gibi altta yatan sağlık sorunları olanlar, RSV’nin neden olduğu ciddi hastalık açısından yüksek risk altındadır” dedi. Değerlendirme ve Araştırma Gümüş Bahar, MarylandFDA’nın duyurusunda.
RSV ARTIŞI, TEKRAR EDEN VAKALARLA İLGİLİ SORULARI ARTIRIR: SİZ VEYA ÇOCUĞUNUZ TEKRAR ALABİLİR MİYİZ?
“Bugün ilk RSV aşısının onaylanması, yaşamı tehdit edebilen bir hastalığı önlemek için önemli bir halk sağlığı başarısıdır ve FDA’nın RSV’nin gelişimini kolaylaştırmaya yönelik devam eden taahhüdünü yansıtmaktadır. güvenli ve etkili aşılar Amerika Birleşik Devletleri’nde kullanılmak üzere” diye devam etti.
Gıda ve İlaç İdaresi (FDA), ABD’de kullanılmak üzere ilk solunum sinsityal virüsü (RSV) aşısını onayladı. (iStock)
Oldukça bulaşıcı olan yaygın bir solunum virüsü olan RSV, Hastalık Kontrol ve Önleme Merkezlerine (CDC) göre genellikle bir veya iki hafta süren hafif, soğuk algınlığı benzeri semptomlara neden olur.
KÜÇÜKLERDE ALT SOLUNUM ENFEKSİYONLARI İLK ERİŞKİN ÖLÜMLERİYLE BAĞLANTILI OLABİLİR: ÇALIŞMA
Yaşlı yetişkinler ve bebekler de dahil olmak üzere bazı yüksek risk gruplarındaki kişiler için virüs daha ciddi koşullara neden olabilir.
Yaşlı erişkinlerde RSV enfeksiyonları akciğer enfeksiyonuna veya pnömoniye yol açabilir ve ayrıca astımı olanlarda komplikasyonlara neden olabilir. kalp hastalığıCDC’ye göre , zayıf bağışıklık sistemleri veya kronik obstrüktif akciğer hastalığı (KOAH).
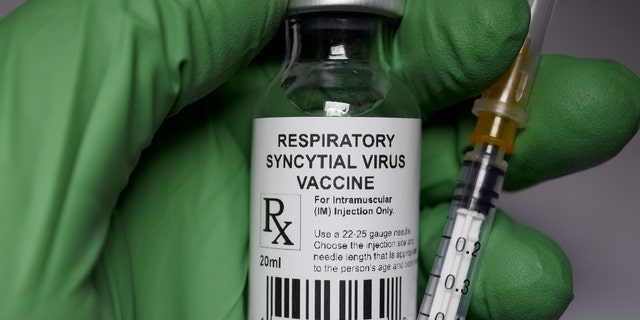
Arexvy (resimde yok) adı verilen ilacın, bir alt solunum yolu hastalığı olan RSV’yi önlemek için 60 yaş ve üzerindeki kişilerde kullanılması onaylandı. (iStock)
CDC, ABD’de her yıl yaklaşık 60.000-160.000 yaşlı yetişkinin RSV ile hastaneye kaldırıldığını ve 6.000-1.000 arasında kişinin virüsten öldüğünü belirtiyor.
Çalışma, aşının ‘kritik faydalarını’ gösterdi
Duyuruya göre FDA, Arexvy’nin 60 yaş ve üstü kişiler için tek bir dozun güvenliğini ve etkinliğini sağlamak için “devam eden, randomize, plasebo kontrollü bir klinik çalışma” yürüttü.
25.000 çalışma katılımcısının yarısı aşı, yarısı plasebo aldı.
FDA, “Aşı, RSV ile ilişkili LRTD (alt solunum yolu enfeksiyonu) geliştirme riskini önemli ölçüde %82,6 oranında azalttı ve ciddi RSV ile ilişkili LRTD geliştirme riskini %94,1 oranında azalttı” dedi.
Fiziksel tıp ve rehabilitasyon doktoru Dr. Shana Johnson, “Bunu bir perspektife koymak gerekirse, aşı grubunda yedi RSV vakası ve plasebo grubunda 40 vaka vardı” dedi. Scottsdale, Arizona’da, Haberler Digital’e söyledi. “Hastaneye yatışlar ve ölüm gibi ciddi hastalıkları azaltmak, kritik faydalardır.”

Yaşlı erişkinlerde RSV enfeksiyonları akciğer enfeksiyonuna veya pnömoniye yol açabilir ve ayrıca astım, kalp hastalığı, zayıflamış bağışıklık sistemi veya kronik obstrüktif akciğer hastalığı (KOAH) olanlarda komplikasyonlara neden olabilir. (iStock)
Çalışmada bildirilen en yaygın yan etkiler enjeksiyon bölgesi ağrısı, kas ağrısı, yorgunluk, eklem ağrısı/sertliği ve baş ağrısıdır.
FDA ayrıca 60 yaş ve üstü yaklaşık 2.500 kişiyi içeren iki küçük çalışma yürüttü.
Katılımcıların hem Arexvy hem de grip aşısı aldığı bu çalışmalardan birinde, iki kişi aşılamadan sonraki yedi ve 22 gün içinde beyin ve omuriliği etkileyen nadir bir iltihaplanma türü olan akut yayılmış ensefalomiyelit (ADEM) geliştirdi.
SAĞLIK BÜLTENİMİZE ÜYE OLMAK İÇİN TIKLAYINIZ
“Daha küçük iki çalışmadan elde edilen güvenlik verilerine dayanarak FDA, şirketin Guillain-Barré ve ADEM’in immün aracılı komplikasyonlarının risklerini kontrol etmek için bir pazarlama sonrası çalışması yapmasını istiyor; bir kişinin başına gelir,” diye açıkladı Johnson.
HABERLER SUNULDU
Johnson, “Şirket ayrıca artan atriyal fibrilasyon (anormal kalp ritmi) oranını değerlendirmeyi taahhüt etti” diye ekledi.
Melissa Rudy, sağlık editörü ve Haberler Digital’de yaşam tarzı ekibinin bir üyesidir.
Arexvy adı verilen ilacın, 60 yaş ve üzerindeki kişilerde bir hastalık olan RSV’yi önlemek için kullanılması onaylanmıştır. alt solunum yolu hastalığı.
FDA Biyoloji Merkezi Direktörü Dr. Peter Marks, “Yaşlı yetişkinler, özellikle kalp veya akciğer hastalığı veya zayıflamış bağışıklık sistemleri gibi altta yatan sağlık sorunları olanlar, RSV’nin neden olduğu ciddi hastalık açısından yüksek risk altındadır” dedi. Değerlendirme ve Araştırma Gümüş Bahar, MarylandFDA’nın duyurusunda.
RSV ARTIŞI, TEKRAR EDEN VAKALARLA İLGİLİ SORULARI ARTIRIR: SİZ VEYA ÇOCUĞUNUZ TEKRAR ALABİLİR MİYİZ?
“Bugün ilk RSV aşısının onaylanması, yaşamı tehdit edebilen bir hastalığı önlemek için önemli bir halk sağlığı başarısıdır ve FDA’nın RSV’nin gelişimini kolaylaştırmaya yönelik devam eden taahhüdünü yansıtmaktadır. güvenli ve etkili aşılar Amerika Birleşik Devletleri’nde kullanılmak üzere” diye devam etti.
Gıda ve İlaç İdaresi (FDA), ABD’de kullanılmak üzere ilk solunum sinsityal virüsü (RSV) aşısını onayladı. (iStock)
Oldukça bulaşıcı olan yaygın bir solunum virüsü olan RSV, Hastalık Kontrol ve Önleme Merkezlerine (CDC) göre genellikle bir veya iki hafta süren hafif, soğuk algınlığı benzeri semptomlara neden olur.
KÜÇÜKLERDE ALT SOLUNUM ENFEKSİYONLARI İLK ERİŞKİN ÖLÜMLERİYLE BAĞLANTILI OLABİLİR: ÇALIŞMA
Yaşlı yetişkinler ve bebekler de dahil olmak üzere bazı yüksek risk gruplarındaki kişiler için virüs daha ciddi koşullara neden olabilir.
Yaşlı erişkinlerde RSV enfeksiyonları akciğer enfeksiyonuna veya pnömoniye yol açabilir ve ayrıca astımı olanlarda komplikasyonlara neden olabilir. kalp hastalığıCDC’ye göre , zayıf bağışıklık sistemleri veya kronik obstrüktif akciğer hastalığı (KOAH).

Arexvy (resimde yok) adı verilen ilacın, bir alt solunum yolu hastalığı olan RSV’yi önlemek için 60 yaş ve üzerindeki kişilerde kullanılması onaylandı. (iStock)
CDC, ABD’de her yıl yaklaşık 60.000-160.000 yaşlı yetişkinin RSV ile hastaneye kaldırıldığını ve 6.000-1.000 arasında kişinin virüsten öldüğünü belirtiyor.
Çalışma, aşının ‘kritik faydalarını’ gösterdi
Duyuruya göre FDA, Arexvy’nin 60 yaş ve üstü kişiler için tek bir dozun güvenliğini ve etkinliğini sağlamak için “devam eden, randomize, plasebo kontrollü bir klinik çalışma” yürüttü.
25.000 çalışma katılımcısının yarısı aşı, yarısı plasebo aldı.
FDA, “Aşı, RSV ile ilişkili LRTD (alt solunum yolu enfeksiyonu) geliştirme riskini önemli ölçüde %82,6 oranında azalttı ve ciddi RSV ile ilişkili LRTD geliştirme riskini %94,1 oranında azalttı” dedi.
Fiziksel tıp ve rehabilitasyon doktoru Dr. Shana Johnson, “Bunu bir perspektife koymak gerekirse, aşı grubunda yedi RSV vakası ve plasebo grubunda 40 vaka vardı” dedi. Scottsdale, Arizona’da, Haberler Digital’e söyledi. “Hastaneye yatışlar ve ölüm gibi ciddi hastalıkları azaltmak, kritik faydalardır.”

Yaşlı erişkinlerde RSV enfeksiyonları akciğer enfeksiyonuna veya pnömoniye yol açabilir ve ayrıca astım, kalp hastalığı, zayıflamış bağışıklık sistemi veya kronik obstrüktif akciğer hastalığı (KOAH) olanlarda komplikasyonlara neden olabilir. (iStock)
Çalışmada bildirilen en yaygın yan etkiler enjeksiyon bölgesi ağrısı, kas ağrısı, yorgunluk, eklem ağrısı/sertliği ve baş ağrısıdır.
FDA ayrıca 60 yaş ve üstü yaklaşık 2.500 kişiyi içeren iki küçük çalışma yürüttü.
Katılımcıların hem Arexvy hem de grip aşısı aldığı bu çalışmalardan birinde, iki kişi aşılamadan sonraki yedi ve 22 gün içinde beyin ve omuriliği etkileyen nadir bir iltihaplanma türü olan akut yayılmış ensefalomiyelit (ADEM) geliştirdi.
Diğer çalışmada, bir kişi, Arexvy ile aşılandıktan dokuz gün sonra, kas zayıflığına ve bazen felce neden olan nadir bir bağışıklık bozukluğu olan Guillain-Barré sendromu geliştirdi.ABD’de her yıl yaklaşık 60.000-160.000 yaşlı yetişkin RSV ile hastaneye kaldırılmaktadır.
SAĞLIK BÜLTENİMİZE ÜYE OLMAK İÇİN TIKLAYINIZ
“Daha küçük iki çalışmadan elde edilen güvenlik verilerine dayanarak FDA, şirketin Guillain-Barré ve ADEM’in immün aracılı komplikasyonlarının risklerini kontrol etmek için bir pazarlama sonrası çalışması yapmasını istiyor; bir kişinin başına gelir,” diye açıkladı Johnson.
HABERLER SUNULDU
Johnson, “Şirket ayrıca artan atriyal fibrilasyon (anormal kalp ritmi) oranını değerlendirmeyi taahhüt etti” diye ekledi.
Melissa Rudy, sağlık editörü ve Haberler Digital’de yaşam tarzı ekibinin bir üyesidir.
